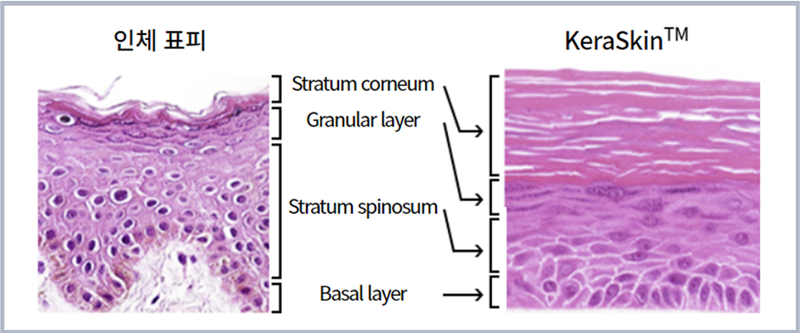
KoCVAMが開発した「KeraSkin」(右)=同ホームページからキャプチャー
[ホン・アンジ]
食品医薬品安全処傘下の食品医薬品安全評価院は27日、国内で開発されたヒト皮膚モデル「KeraSkin」を用いた光毒性の動物代替試験法が、OECD第38回試験ガイドライン(TG498)に採択されたと発表した。
韓国動物代替試験法検証センター(KoCVAM)が開発したこの試験法は、外国産モデルへの依存から脱却した韓国独自の技術である。ヒト皮膚モデルを活用し、化粧品原料などの光毒性を評価するもので、動物実験の代替となる革新的な手法とされる。
今回の採択は、23日に開催されたOECD国家試験指針プログラム調整者作業部会(WNT)で決まった。KeraSkinはOECD加盟38カ国のうち、米国のモデルに続き世界で2例目のヒト皮膚モデルとして登録された。
産業面での価値も大きい。国内の化粧品業界では、高価な海外製モデルの使用に伴う試験費用や輸送時間を大幅に削減できるようになる。さらに、韓国人の肌に適した安全性データを確保することで、海外市場への進出も加速する見通しだ。
食品医薬品安全処は「化粧品政策の現場において動物代替試験法が定着するよう、制度的支援を強化する」と強調した。
shong9412@korea.kr